Stabilisierung von Proteinen durch Polymere

100 Jahre Makromolekulare Chemie
Proteine kommen in der Natur in vielfältiger Form vor: Enzyme katalysieren Reaktionen, Proteinkanäle ermöglichen selektiven Transport, Strukturproteine geben Form und Stabilität. Der einzigartige Aufbau und die spezifischen Funktionen von Proteinen lassen sich mit synthetischen Polymeren nicht nachahmen. Stattdessen rückt es verstärkt in den Fokus aktueller Forschung, Proteine mit ihren herausragenden Funktionen zu nutzen. Dies spiegelt sich in der sogenannten Biologischen Transformation und dem verstärkten Fokus auf Bioökonomie wider. Bisher ist eine konsequente Verwendung von Proteinen dadurch limitiert, dass Proteine in nicht-natürlicher Umgebung eine deutlich verringerte Stabilität aufweisen. Das heißt, ihre Löslichkeit ist geringer, sie aggregieren verstärkt und fallen aus oder haben schlichtweg nicht mehr ihre ursprüngliche Form und damit einhergehend nicht mehr ihre Funktion. Durch kovalentes Anbinden von synthetischen Polymeren lassen sich Proteine stabilisieren, so dass ihre Löslichkeit erhöht und ihr Funktionsverlust minimiert wird.
Synthese von Protein-Polymer-Konjugaten
Bei der Synthese von Protein-Polymer-Konjugaten werden zwei Ansätze unterschieden, die man als grafting-to und grafting-from bezeichnet. [1] Bei ersterem wird das Polymer zunächst individuell synthetisiert und anschließend an das Protein gebunden. Bei grafting-from wird dagegen ein Initiator oder Kettenüberträger für eine Polymerisation an ein Protein gebunden und das Polymer wächst im nächsten Schritt von der Oberfläche des Proteins weg. Um dabei die Löslichkeit des Proteins zu gewährleisten, muss die Polymerisation in einer wässrigen Pufferlösung durchgeführt werden.
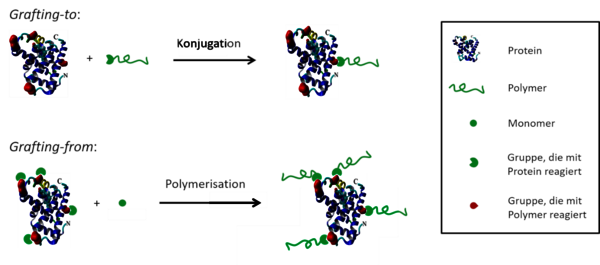
Schema der grafting-to und grafting-from Strategien zur Synthese von Protein-Polymer-Konjugaten. © Johannes Martin, Ulrich Glebe
In beiden Ansätzen erfolgt die kovalente Modifizierung der Proteine üblicherweise an den Lysin- oder Cystein-Resten sowie den N- oder C-Termini. Entsprechend funktionalisierte Initiatoren und Kettenüberträger (für grafting-from) sowie Polymer-Endgruppen (für grafting-to) zur selektiven Anbindung wurden und werden weiterhin entwickelt. [2]
Beide Strategien haben ihre intrinsischen Vor- und Nachteile:
| Grafting-to | Grafting-from |
| + Kontrollierte Polymersynthese | – Unkontrollierte Polymersynthese führt zu breiter Molekulargewichtsverteilung |
| + Leichte Charakterisierung der Polymere | – Charakterisierung der Polymere schwierig |
| – Anbindung von Makromolekülen sterisch und thermodynamisch ungünstig: niedrige Ausbeute und geringe Anzahl an Polymerketten pro Protein | + Keine sterische Hinderung bei Synthese: viele Polymerketten pro Protein möglich |
| – Reinigung des Konjugats von unmodifiziertem Protein und überschüssigem Polymer schwierig | + Leichte Reinigung: ausschließlich kleine Moleküle (verbleibende Monomere und eventuell Katalysator) leicht zu entfernen |
Protein-Polymer-Konjugate für therapeutische Anwendungen
Das Hauptanwendungsgebiet von Protein-Polymer-Konjugaten liegt in der Pharmazie. Viele Proteine sind therapeutisch wirksam und werden gegen Krankheiten wie Krebs, Hepatitis oder Autoimmunerkrankungen eingesetzt. Jedoch sind viele unmodifizierte Proteine im Körper nur bedingt stabil und werden schnell durch das Immunsystem angegriffen. Deshalb liegt das Hauptziel in der Entwicklung von Protein-Polymer-Konjugaten darin, die in vivo Halbwertszeit des jeweiligen Proteins zu verlängern, um dadurch die Dosis und die Anzahl der Verabreichungen zu verringern. Seit den 1970er-Jahren wurden PEGylierte Proteine entwickelt, bei denen die angebundenen Poly(ethylenglykol)-Ketten zu einer Stabilisierung führen. Obwohl Protein-PEG-Konjugate meistens eine verringerte Aktivität im Vergleich zu dem unmodifizierten Protein haben, führt die deutlich verlängerte Verweildauer im Körper zu einer insgesamt verbesserten Wirkungsweise des therapeutischen Proteins. Daher lohnen sich die hohen Entwicklungskosten bis zur Medikamentenzulassung für die Konjugate. [3]
Weiterhin besteht Forschungsbedarf
Viele der zugelassenen PEGylierten Arzneimittel sind eine Mischung unterschiedlicher Spezies. Die PEG-Ketten sind beispielsweise an unterschiedliche Lysin-Reste gebunden. Viele Konjugate mit ortsspezifisch angebundenen Polymeren haben eine bessere Wirkung; ihre Aktivität ist nämlich dann höher, wenn die Polymere weiter entfernt von dem aktiven Zentrum des Proteins angebunden sind. So wurden in den letzten Jahren Konjugate mit besserer Wirkung als bereits zugelassene Medikamente entwickelt. Den optimierten Konjugaten steht aber noch ein jahrelanger Zulassungsprozess bevor.
Während sich Proteine biotechnologisch in Standard-Verfahren verändern und optimieren lassen, ist dieser Prozess bei Protein-Polymer-Konjugaten wesentlich aufwändiger: viele Einflussfaktoren sind nicht generalisierbar und müssen nach tagelanger Synthese einzeln untersucht werden. [4] So lassen sich Position, Anzahl, Länge und Art des verwendeten Polymers variieren. Nachdem einige Patienten Antikörper gegen PEG entwickelt haben, wird vermehrt an alternativen Polymeren geforscht. Weiterer Verbesserungsspielraum besteht darin, neben der in vivo Halbwertszeit auch die Lagerungsstabilität von Proteinen zu erhöhen.
Neben biomedizinischen Anwendungen versprechen Konjugate auch in anderen Gebieten Innovationspotential: Membranproteine könnten als einheitliche Nanoporen in Membranen eingesetzt werden, künstliche Zellen sind denkbar und Enzyme könnten viele Funktionen übernehmen, für die jetzt noch anorganische Katalysatoren verwendet werden. In all diesen Fällen könnte die Stabilisierung der Proteine durch Polymere eine entscheidende Rolle spielen.
Autoren: Dr. Ulrich Glebe und Prof. Dr. Alexander Böker (Fraunhofer-Institut für Angewandte Polymerforschung IAP)
Redaktionelle Bearbeitung: Lisa Süssmuth, GDCh
Literatur
[1] U. Glebe, B. Santos de Miranda, P. van Rijn, A. Böker, in Bio-Synthetic Hybrid Materials and Bionanoparticles: A Biological Chemical Approach Towards Material Science, RSC Smart Materials No. 16, 2015, 1-29.
[2] B. Jung, P. Theato, Adv. Polym. Sci. 2013, 253, 37-70.
[3] J. H. Ko, H. D. Maynard, Chem. Soc. Rev. 2018, 47, 8998-9014.
[4] A. J. Russell, S. L. Baker, C. M. Colina, C. A. Figg, J. L. Kaar, K. Matyjaszewski, A. Simakova, B. S. Sumerlin, AIChE J. 2018, 64, 3230-3245.

Kommentare
Keine Kommentare gefunden!