Was ist eigentlich... Alkohol?

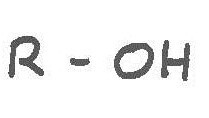
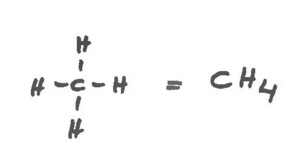
Was charakterisiert den Alkohol? Dass er beschwipst macht und man möglicherweise sogar die Kontrolle über sich selbst verliert? Chemikerinnen und Chemiker sehen das anders. Sie sagen: Alkohole – es gibt nämlich nicht nur einen – sind Kohlenwasserstoffe mit einer oder mehreren Hydroxy(-OH)-gruppen und machen es sich in der Formelsprache einfach. Sie bezeichnen Alkohole einfach nur als R-OH. „R“ ist die Abkürzung von „Rest“, einer ungeheuren Vielzahl von Kohlenwasserstoffen.
Kompliziert? Keineswegs! Kohlenwasserstoffe sind auf der Erde weit verbreitet. Sie bestehen aus Kohlenstoff(C)- und Wasserstoff(H)-Atomen. Der einfachste Kohlenwasserstoff ist Methan (CH4), der Hauptbestandteil des Erdgases. Das C-Atom ist hierin von vier H-Atomen umgeben.
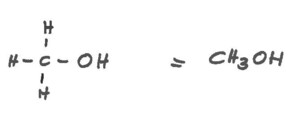
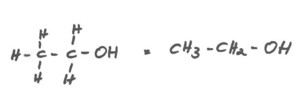
Ersetzt man nun ein H-Atom durch eine Hydroxy(-OH)-gruppe so hat man schon den einfachsten Alkohol: Methanol (CH3OH). Doch den sollte man tunlichst nicht trinken. Er führt zu Blindheit und sogar zum Tod, wie tragische Vorfälle immer wieder zeigen!
Anders der zweiteinfachste Alkohol, Ethanol – unser „Spiritus“ oder „Weingeist“. Ethanol ist das, was wir umgangssprachlich unter „Alkohol“ verstehen. Ethanol hat nur ein Kohlenstoff-Atom mehr als Methanol. CH3CH2OH heißt die Molekül-Formel dieses Alkohols, den wir mit Bier und Wein, Wodka und Rum, kurz mit allen alkoholischen Getränken konsumieren. Blind macht er nur so manchen Alkoholiker vor der Gefahr, die ihm dieser Alkohol tatsächlich langfristig auch bringen kann: den Tod – aber sehr viel schleichender als beim unmittelbar wirkenden Methanol. Wir rekapitulieren:
Der einfachste Alkohol ist das giftige Methanol, CH3OH, früher auch Holzgeist genannt, dann folgt unser „Glücksbringer“ Ethanol, C2H5OH, und als nächster Propanol mit insgesamt drei Kohlenstoffatomen. Hier gibt es bereits zwei Strukturen mit unterschiedlichen Eigenschaften, nämlich Propanol CH3-CH2-CH2-OH und Isopropanol CH3-CHOH-CH3.
Wie können Alkohole entstehen?
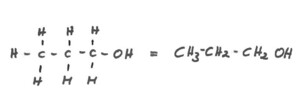
Propanol
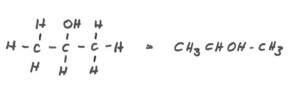
Isopropanol
Zum Beispiel durch Vergärung zuckerhaltiger Agrarprodukte wie Trauben, Obst, Rüben und Getreide. Die Vergärung selbst wird von Hefepilzen übernommen, die sich von Zucker ernähren und als Stoffwechselprodukt Alkohole produzieren. Dieser Vorgang ist auch die Basis für die Herstellung von Bioethanol. Aktuell ist es für die Chemie eine große Herausforderung, effiziente Wege für die Herstellung von Bioethanol zu finden. Diesen möchte man nämlich nicht aus Nahrungsmitteln wie z.B. Mais, sondern Cellulose gewinnen, da Cellulose für die Ernährung nicht verwendet wird. Neben der Vergärung gibt es auch technische Verfahren auf der Basis von Erdöl, um Alkohole herzustellen.
Die meisten Alkohole sind gute Lösemittel. Denn ihr „R“ der Kohlenwasserstoffe löst nach dem Motto „Gleiches in Gleichem“ eine Vielzahl von organischen Substanzen. Die Hydroxygruppe [-OH] sorgt dagegen dafür, das sich Alkohole auch in Wasser lösen – Gott sei Dank! Sonst könnten wir ja nur 100%ige Schnäpse trinken – der Wein mit 12 Prozent (Alkohol in Wasser) bliebe uns vorenthalten. Auf den trinkbaren Alkohol, das Ethanol, müssen Steuern bezahlt werden. Unbesteuertes Ethanol für technische Zwecke wird vergällt, um Missbrauch vorzubeugen. Das bedeutet, ihm werden Stoffe beigemischt, damit man ihn nicht mehr trinken kann.
Und wofür sonst braucht man all diese und noch exotischere Alkohole?
Alkohole spielen in der Chemie eine wichtige Rolle. Sie finden für Geruchs- und Geschmacksstoffe in der Lebensmittel- und Parfümindustrie Verwendung, Geraniol beispielsweise ist ein angenehm nach Rosen duftendes Öl. Alkohole dienen auch als Lösemittel für Farben und Lacke oder für Duftstoffe im Parfüm oder Wirkstoffe in flüssigen Arzneien. Durch Oxidation von Alkoholen können sich Carbonsäuren bilden, z.B. aus Ethanol Essigsäure CH3COOH. So wird auch der Wein, durch Oxidation mit Sauerstoff aus der Luft, vom langen Stehen sauer, ausgetrunken will er sein, wie es im Hermann-Löns-Lied heißt.
Der Beitrag wurden vom Arbeitskreis Öffentlichkeitsarbeit der Seniorexperten Chemie, einer Fachgruppe der Gesellschaft Deutscher Chemiker, erstellt.
Autorinnen: Dr. Renate Hoer, Dr. Ursula Kraska (bearbeitet durch kjs)
In der Reihe „Was ist eigentlich…“ stellen wir in leicht verständlicher Form chemische Substanzen vor, die jeder kennt oder fast jeder benutzt. Alle Beiträge der Reihe: https://faszinationchemie.de/chemie-ueberall

Kommentare
Ichmagalkohol
am 03.02.2022Hans Blumenstock
am 01.11.2022ich hätte noch etwas über das Zwischenprodukt Acetaldehyd (Ethanal) wegen seiner besonderen gesundheitlichen Gefährlichkeit hinzugefügt
H. Blumenstock
kjs (Redaktion)
am 01.11.2022Paul
am 14.03.2024kjs (Redaktion)
am 15.03.2024